Biokimia Nutrisi (Ekskresi Nitrogen dalam Urin)
Tinjauan pustaka
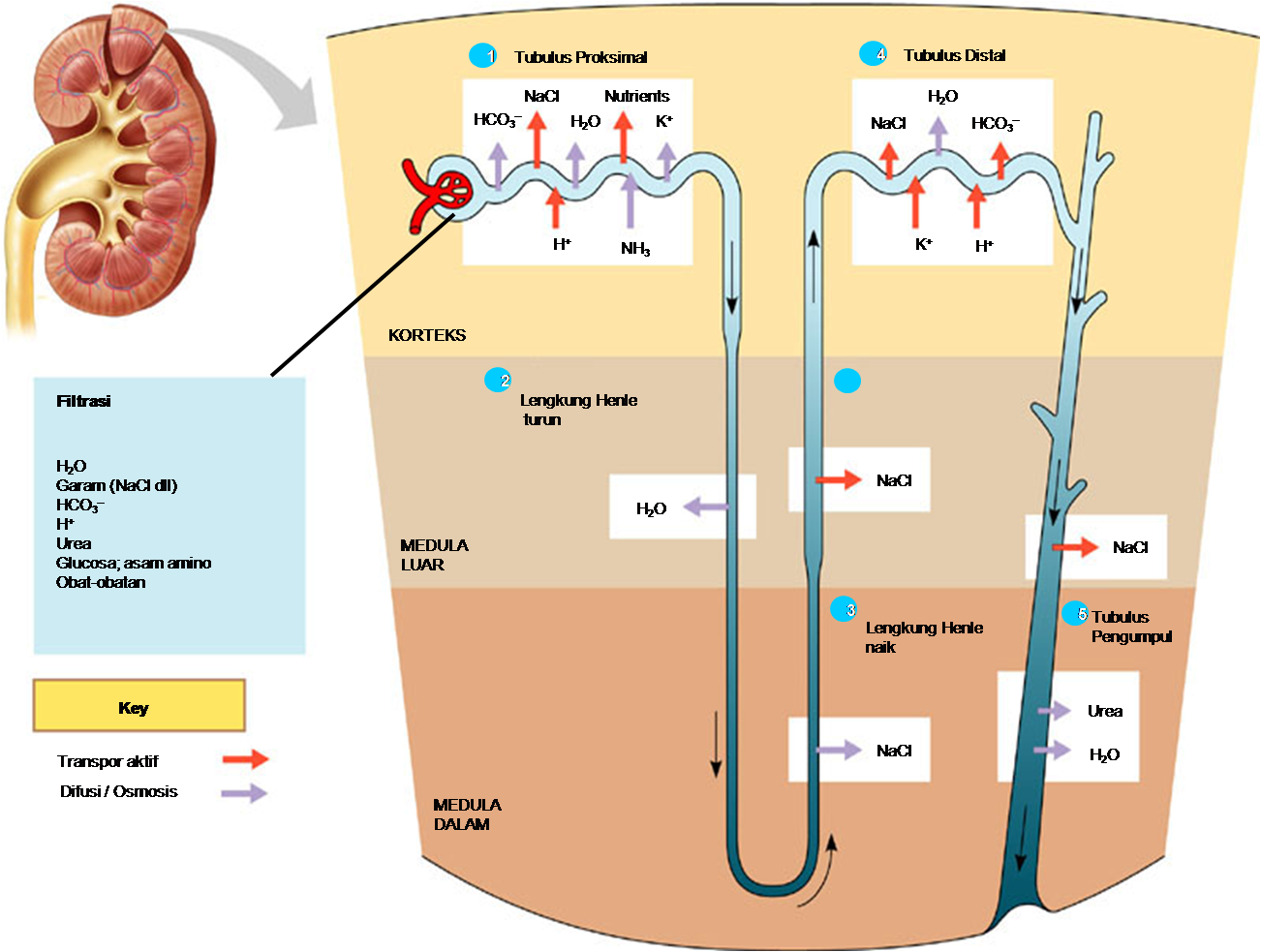 |
| Klik gambar untuk memperbesar |
Nitrogen yang merupakan unsur terpenting semua organisme, dalam binatang
dalam berntuk nitrogen protein dan nitrogen non protein (NPN). Senyawa nitrogen
dapat berasal dari pakan dan endogen yang berupa urea saliva (Perry, 1984).
Protein dan NPN pada ternak ruminansia mempunyai fungsi antara lain untuk
membangun dan menjaga protein jaringan tubuh, menyediakan asam-asam amino,
menyediakan sumber-sumber energi dan sumber lemak tubuh, sumber glikogen darah,
penyusun enzim-enzim tubuh, penyusun hormone tubuh, serta menyediakan komponen
tertentu dari DNA (Tilman et al.,
1991).
NH3 yang tidak digunakan
untuk sintesis protein akan diabsorbsi kembali melalui pembuluh darah menembus
dinding rumen menuju siklus urea di dalam hati, melalui siklus urea tersebut
sebagian kecil akan masuk kembali kedalam rumen melalui saliva atau langsung
menembus dinding rumen melalui pembuluh darah dan digunakan lagi sebagai sumber
Nitrogen, sedangkan bagia urea akan difiltrasi oleh ginjal dan akhirnya
diekskresikan lewat urin (Van Soest, 1994).
Ekskresi N lewat urin yang
tinggi disebabkan karena tidak seimbangnya degradasi protein sebagai sumber N
dan fermentasi karbohidrat didala rumen sebagai sumber energi untuk sintesis
mikroba (Tamminga et al., 1990).
Hilangnya N melalui feses diakibatkan oleh ekresi N pakan yang tidak tercerna
dan N endogen (Tamminga, 1992).
Materi dan metode
Materi
Alat. yang digunakan pada praktikum kali ini
adalah labu ukur, pemanas api, alat destruksi, Erlenmeyer, penampung, labu
kajeldahl, alat pendingin, alat destilasi, buret, sentrifuge, pemvortek,
inkubator.
Bahan. Bahan yang
digunakan dalam praktikum kali ini adalah urin, H2SO4,
katalisator (CuSO4:K2SO4= 1:2), H3BO3,
aquadest, indicator mix, indicator PP, NaOH, Zn logam.
Metode
Penentuan kadar N total dengan
metode kajeldahl. Preparasi
sampel berupa 1 ml urine, 4 ml H2SO4 dan 3
gram katalisator yaitu berupa CU2SO4 dan K2SO4
dengan perbandinagan 1:2. sampel tersebut dimasukkan dalam labu dan
dilakukan Destruksi, Destilasi dan Titrasi. Untuk destruksi labu yang berisi
sampel dimasukkan atau diletakakn dalam pemanas dengan api kecil. Ketika sampel
dipanaskan larutan akan berubah warna menjadi hitam, dan labu segera diputar
pelan-pelan hingga warna menjadi jernih kembali dan tidak terlihat adanya asap.
Setelah warna jernih bertahan selama 1 jam destruksi dihentikan.
Setrelah di destruksi maka
dilanjutkan proses destilasi yaitu dengan mengencerkan sampel hasi destruksi
hingga 50 ml, sampel ini didiamkan dahulu sampai dingin. Kedalam erlenmeyer
ukuran 100 ml ditambahkan 20 ml H3BO3 0,1 N dan 20 ml
aquades dan 3 tetes indikator mix. Setelah itu ditambahkan dengan indikator
mix. Setelah itu dititrasi dengan HCl 0,2 N hingga berubah warna. Kemudian di
hitung dengan rumus:
Kadar N dalam
urin = (X-Y) x N x 0,014 X 100%
Z
X = HCl titrasi
sampel, Y titrasi blanko, Z jumlah sampel
Hasil dan pembahasan
Penentuan kadar N total dengan
metode kajeldahl. Dalam penentuan kadar N total dalam urin digunakan
preparasi sampel berupa 1 ml urine, 4 ml H2SO4 dan 3 gram katalisator yaitu berupa CU2SO4 dan K2SO4 dengan
perbandinagan 1:2. sampel tersebut dimasukkan dalam labu dan dilakukan
Destruksi, Destilasi dan Titrasi. Untuk destruksi labu yang bverisi sampel
dimasukkan atau diletakakn dalam pemanas dengan api kecil. Fungsi dari H2SO4 ini akan
bekerja aktif saat dipanaskan. Begitu pula dengan katalisator. Jika sampel
dipanaskan maka reaksi akan berlangsung
cepat dan dengan penambahan H2SO4 maka nitrogen akan terlapas. Ketika sampel dipanaskan
larutan akan berubah warna menjadi hitam, dan labu segera diputar pelan-pelan
hingga warna menjadi jernih kembali dan tidak terlihat adanya asap. Setelah
warna jernih bertahan selama 1 jam destruksi dihentikan.
Setelah di destruksi maka
dilanjutkan proses destilasi yaitu dengan mengencerkan sampel hasi destruksi
hingga 50 ml, sampel ini didiamkan dahulu sampai dingin. Kedalam erlenmeyer
ukuran 100 ml ditambahkan 20 ml H3BO3 0,1 N dan 20 ml aquades dan 3 tetes indickator mix.
Hasil destruksi berikatan dengan H2SO4 membentuk amoniumsulfat dan dilakukan destilasi dengan
penambahan NaOH akan terbentuk ammonium sulfat dan membentukj amoniak. Saat
dialiri pendingin amoniak akan menguap, ketika menguap amoniuak akan menetes
kedalam Erlenmeyer yang sudah berisi H3BO3 amoniak tersebut ditangkap oleh H3BO3 dan
warna berubah menjadi hijau. Setelah itu ditambahkan dengan indicator mix dan
warna menjadi ungu. Setelah itu dititrasi dengan HCl 0,2 N. HCl ini digunakan
sebagai indicator apakah sifat basa sudah hilang. Setalah dititrasi warna
larutan menjadi hijau kembali. HCl titrasi sempel dalam praktikum kali ini
sebesar 1,86 dengan titrasi blangko senilai 0.06 dan sempel yang digunakan
ialah 20. dari hasil perhitungan didapatkan kadar N urin sebesar 0,013734.
Kesimpulan
Penentuan kadar N total dengan
metode kjeldahl melalui 3 tahap yaitu destruksi, destilasi, dan titrasi. Pada
tahap destruksi dengan adanya katalisator akan mempercepat reaksi. Dan saat
destilasi penambahan H3BO3 dan indikator mix membuat warna larutan berubah menjadi
ungu dan pada titrasi karma penambahan HCl membuat warna larutan menjadi hijau.
Dengan tahap-tahap tersebut dapat diketahui kadar N yaitu sebesar 0,013734.
Daftar pustaka
Perry, T.W. 1984. Animal
life cycle. Feeding and Nutrition. Academic press. New York.
Tamminga, S. A. M Van Vuuren, C. J. Van de Koelen , R.S Katalar and P. L
Van den Togh. 1990. Ruminal
Behavior of Structural Ingredients in Dairy Cows. J. Agr sci.38=513.
Tamminga, S. 1992.
Nutrition Management of Dairy Cows as Contribution to Pollution Control.
J.Dairy sci 75= 345-357.
Tillman et all. 1998. Ilmu Makanan Ternak Dasar. Gadjah Mada University Press :
Yogyakarta.
Van Soest, P. J. 1994.
Nutritional Ecology of the Ruminant 2nd ed. Comstock Publishing
Associates, A Division of Cornel University Press, Ithaca and London.
Lampiran
Penentuan kadar N dengan metode kjeldahl
Diketahui Ts =
1,86
Tb =
0,04
N HCl =
0,1090
BA.N =
14,008
Ditanyakan kadar N
Jawab
Kadar
N = 50 x ts – tb x N
HCl x BA.N x 100%
20
1000
= 50 x 1,86 – 0,04 x
0,1090 x 14,008 x 100%
20
1000
= 2,5 x 0,00182 x 0.1090 x 14,008 x
100%
= 0,00695 x 100%
= 0,695 mg/dl
Comments
Post a Comment